Prisbelönt leverforskning
2015-11-04 / Svensk Kirurgi / Volym 73 / Nr 5 / 2015
Med stor glädje mottog jag beskedet att jag utsetts till Bengt Ihre-stipendiat 2015, och jag vill tacka Svensk Kirurgisk Förening och Bengt Ihre-stiftelsen för äran. Sedan 2006 arbetar jag vid Skånes Universitetssjukhus i Lund där jag är överläkare vid sektionen för lever-, pankreas- och gallvägskirurgi och docent i kirurgi vid Lunds universitet. Min forskning som uppmärksammats via stipendiet rör kirurgisk behandling av kolorektala levermetastaser och inverkan av preoperativ cellgiftsbehandling på leverns regeneration och funktion.

Christian Sturesson
christian.sturesson@med.lu.se
Lund
Som heltidsarbetande kirurg, med många patienter att operera och ännu fler att bedöma på multidisciplinära team-konferenser, ges möjlighet att se mönster i sjukdomsförlopp. Mönster som inte alltid har registrerats eller rapporterats tidigare. Dessutom finns det i den kliniska vardagen dagligen problem att hantera. Om problemen upprepas är det naturligt att försöka identifiera gemensamma faktorer för att kunna sätta in åtgärder, även om det kan vara svårt att helt förstå orsakssambanden. Mina forskningsidéer kommer ofta från igenkänning av mönster, där jag för problemanalys gärna kombinerar känd kunskap på ett nytt sätt.
Kliniska frågeställningar
De forskningsfrågor jag vill besvara har alla sitt ursprung i kliniska problem från den kirurgiska vardagen. En vardag jag tränats för först i allmänkirurgi i Eksjö med goda kliniska lärare, främst Karsten Offenbartl och Per Gullstrand, och därefter i Lund med Per Jonas Blind som oslagbar mentor i lever- och pankreaskirurgi. Efter en dags opererande gick Per Jonas och jag ofta till sjukhusgymmet för en duell pingis samtidigt som vi bollade forskningsidéer och diskuterade kirurg-tekniska problem. Nedan följer några exempel på genomförda forskningsprojekt.
Regeneration
Vid kirurgisk behandling av levertumörer är det avgörande att den lever som lämnas kvar efter resektion har tillräcklig funktion för att undvika postoperativ leversvikt och tilllåta regeneration. Exakt var den gränsen går är idag svår att förutse men i praktiken sparas minst 30 procent av ursprunglig levervolym. Vid kolorektala levermetastaser ges ofta preoperativ cellgiftbehandling, antingen som neoadjuvant eller konverteringsbehandling, då detta har visat sig ha positiva onkologiska effekter. Cellgiftbehandlingens effekt på levervävnaden är då av intresse och vi har visat att cellgiftsbehandling medför försämrad regeneration efter både resektion och portavensocklusion(1,2). Portavensocklusion innebär att man fyra–sex veckor före resektion stoppar portaflödet till den av levern som senare ska opereras bort vilket leder till tillväxt av den del som ska vara kvar. Tillväxthämningen är liten men signifikant. Resultatet har upprepats vid sammanläggning av vårt material med det från Amsterdam(3) .
Mikrocirkulation
Hösten 2011 tillbringade jag vid Academisch Medisch Centrum i Amsterdam under ledning av professor Thomas van Gulik för att vidareutveckla mina idéer kring portavensocklusion och för att utvärdera ett instrument för intraoperativ mätning av mikrocirkulation i levern. Tidigare experimentella studier har visat att till exempel leversteatos leder till sämre mikrocirkulation vilket kan vara en orsak till den steatotiska leverns sämre funktion. Efter experimentell validering av instrumentet, som baserades på laser speckle teknik(4) , ledde jag i Lund en klinisk pilotstudie(5). Det stod snart klart att det krävs ytterligare mjukvaruutveckling innan instrumentet kan användas för tillförlitliga kliniska mikrocirkulationsmätningar. Min forskargrupp har även undersökt leverns mikrocirkulation med ett handhållet mikroskop och har, för första gången på människa, kunnat kvantifiera hastighetsökningen av blod i sinusoiderna efter leverresektion(6). Tekniken förutsåg även histologiska skador på levervävnaden.
Ny peroperativ diagnostik
Jag har gått vidare med projekt kring intraoperativ mätning av leverfunktion. Då man som leverkirurg ser en blåaktigt missfärgad lever som följd av cellgiftsbehandling blir man bekymrad över leverns funktion. För närvarande finns inte någon tillförlitlig metod för preoperativ identifiering av dessa patienter. Vid leversteatos, som kan vara en annan följd av cellgiftsbehandling, ser levern mer gul ut. Dessa för ögat synliga förändringar fick mig att fundera på om kvantifiering av leverns färg kan ge information om dess funktion. Med en doktorstitel i fysik i bagaget hade jag idéer om hur detta kunde mätas. Docent Nina Reistad på Lunds tekniska högskola har nu byggt ett instrument som gör just detta, baserat på diffus reflektansspektroskopi. Instrumentet belyser leverytan med vitt ljus och registrerar det ljus som återvänder till proben efter att ljuset växelverkat med levervävnaden. Ljuset våglängdsuppdelas och skillnaden mellan insänt och reflekterat ljus ger då en profil av leverns molekylära sammansättning. Hittills har vi studerat ett 40-tal patienter och preliminärt får vi korrelation mellan den histologiska bilden och uppmätta spektra. Tekniken skulle även kunna användas för kvantifiering av leverfunktion vid levertransplantation.
Tvåstegsoperation överflödigt?
Ett annat problem vid portavensocklusion är om det finns tumörer i den del av levern som ska tillväxa. Farhå- gor finns att portavensocklusion kan leda till tumörtillväxt som omöjliggör radikaloperation, och dessa patienter behandlas därför ofta med så kallad tvåstegsoperation. Vid första operationen tas tumörerna bort i den del som ska tillväxa och portavensockludering utförs. Efter fyra–sex veckor görs så en andra operation med fullständig tumörresektion. Jag kunde dock notera att våra patienter som portavensockluderats under samtidig cellgiftsbehandling inte syntes uppvisa någon tumörtillväxt under regenerationsfasen. Genom att lägga samman vårt material med det från Huddinge kunde vi visa att så var fallet(7). Således kan flera av dessa patienter undvika en av två operationer.
Komplett tumörrespons ovanligt
Riskfaktorer för ärrbråck
Förbättrad forskningsmiljö
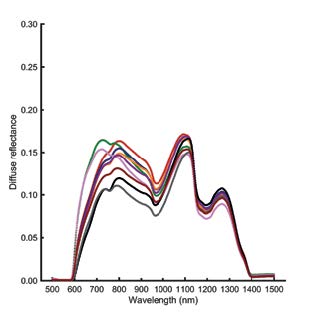
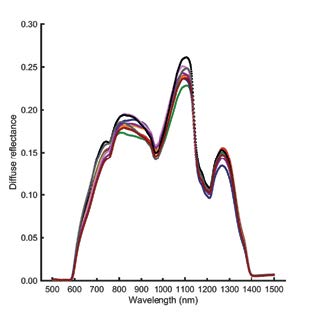
Diffus reflektansmätningar på normal lever (till vänster) och steatotisk lever (till höger). Man kan se skillnad mellan detekterat ljus vid 1200 nm där fett absorberar och 1100 nm där vävnadsabsorptionen är låg. Figurerna inkluderar nio separata mätningar över leverytan.
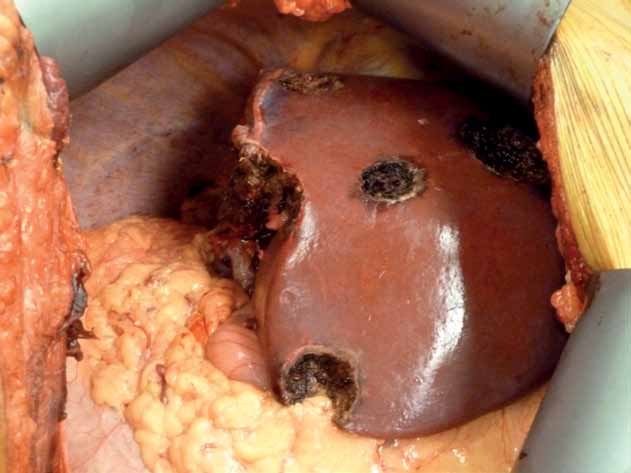
Resultat efter utvidgad högersidig leverresektion med multipla lokala resektioner fem veckor efter perkutan högersidig portavensembolisering.
Referenser
1. Sturesson C, Keussen I, Tranberg KG. Prolonged chemotherapy impairs liver regeneration after portal vein occlusion – an audit of 26 patients. Eur J Surg Oncol 2010;36(4): 358-364.
2. Sturesson C, Nilsson J, Eriksson S, Spelt L, Andersson R. Limiting factors for liver regeneration after a major hepatic resection for colorectal cancer metastases. HPB (Oxford) 2013;15(8): 646-652.
3. Sturesson C, Hoekstra L, Andersson R, van Gulik TM. Importance of thrombocytes for the hypertrophy response after portal vein embolization. Hepatogastroenterology 2015;62(137): 98-101.
4. Sturesson C, Milstein DM, Post IC, Maas AM, van Gulik TM. Laser speckle contrast imaging for assessment of liver microcirculation. Microvasc Res 2013;87: 34-40.
5. Eriksson S, Nilsson J, Lindell G, Sturesson C. Laser speckle contrast imaging for intraoperative assessment of liver microcirculation: a clinical pilot study. Medical devices 2014;7: 257-261.
6. Nilsson J, Eriksson S, Blind PJ, Rissler P, Sturesson C. Microcirculation changes during liver resection–a clinical study. Microvasc Res 2014;94: 47-51.
7. Spelt L, Sparrelid E, Isaksson B, Andersson RG, Sturesson C. Tumour growth after portal vein embolization with pre-procedural chemotherapy for colorectal liver metastases. HPB (Oxford) 2015;17(6): 529-535.
8. Sturesson C, Nilsson, J., Lindell, G., Andersson, R., Keussen I. Disappearing liver metastases from colorectal cancer – impact of modern imaging modalities. HPB 2015;accepted for publication.
9. Nilsson J, Holka, P, Sturesson, C. Incisional hernia after open resections for colorectal liver metastases – incidence and risk factors. Submitted
10. Blind PJ, Andersson B, Tingstedt B, Bergenfeldt M, Andersson R, Lindell G, Sturesson C. Fast-track program for liver resection–factors prolonging length of stay. Hepatogastroenterology 2014;61(136): 2340-2344.
11. Williamsson C, Karlsson N, Sturesson C, Lindell G, Andersson R, Tingstedt B. Impact of a fast-track surgery programme for pancreaticoduodenectomy. Br J Surg 2015;102(9): 1133-1141.
